41. Wissenschaftliche Jahrestagung der Deutschen Gesellschaft für Phoniatrie und Pädaudiologie (DGPP)
41. Wissenschaftliche Jahrestagung der Deutschen Gesellschaft für Phoniatrie und Pädaudiologie (DGPP)
Erhöhte Pneumonie-Inzidenz bei Dysphagie-Patienten nach Schlaganfall mit oraler Nahrungskarenz
Abstract
Hintergrund: Dysphagie-Patienten haben ein erhöhtes Risiko für eine Schlaganfall-assoziierte Pneumonie (SAP), die mit einer höheren Sterblichkeit und schlechterem neurologischem Outcome korreliert. Die Wahrscheinlichkeit einer SAP wird durch die Faktoren Alter, Vorhofflimmern, Dysphagie, männliches Geschlecht und Schwere des Schlaganfalls beeinflusst, die im A2DS2-Score erfasst werden. Ziel unserer bizentrischen Studie war es, die Auswirkung diätetischer Einschränkungen, insbesondere nil per os (NPO) und texturmodifizierte Kost (TMF), auf die SAP-Inzidenz bei Dysphagie nach Schlaganfall zu untersuchen.
Material und Methoden: Die Daten von 160 konsekutiven Patienten wurden retrospektiv ausgewertet: 73 Männer (Spanne 22–95 Jahre, Median 79) und 87 Frauen (Spanne 50–101 Jahre, Median 84). Die Betroffenen wurden auf zwei Schlaganfallstationen mit einer Gesamtkapazität von jeweils 20 Betten behandelt. Das primäre Outcome war die SAP-Inzidenz, während die Dauer des Krankenhausaufenthalts, die Sterblichkeit und die Notwendigkeit einer nasogastralen Sondenanlage zu den sekundären Outcomes gehörten.
Ergebnisse: Die Ergebnisse zeigten eine starke Korrelation zwischen dem A2DS2-Score und der SAP-Wahrscheinlichkeit (p<0,001). Die Schwere des Schlaganfalls, männliches Geschlecht und Alter waren signifikante SAP-Risikofaktoren. Bei Aufnahme erhielten 63% der SAP-Patienten bereits NPO, 33,3% TMF, und nur 3,7% hatten keine Einschränkungen bei der oralen Nahrungsaufnahme. NPO-Patienten hatten ein 2,5-mal höheres Risiko, eine SAP zu entwickeln als Patienten ohne Ernährungseinschränkungen (p=0,008). Die Mehrzahl der SAP-Diagnosen wurde vor Beginn der oralen Nahrungsaufnahme gestellt, wobei die meisten Fälle bis zum dritten Tag entdeckt wurden.
Schlussfolgerungen: Trotz NPO zur Vorbeugung von Lungenentzündungen entwickelten viele Patienten dennoch eine SAP, was auf einen Einfluss von Mundhygienefaktoren und/oder systemischen und lokalen Immunveränderungen auf die pulmonale bakterielle Abwehr hindeutet. Unsere Studie unterstreicht die Notwendigkeit eines frühzeitigen Eingreifens und umfangreicher Pflegestrategien zur Minderung des SAP-Risikos bei Dysphagie-Patienten nach Schlaganfall. Geeignete Dysphagie-Diäten, die das residuale Schluckvermögen verbessern, könnten sowohl die SAP-Raten als auch die Dysphagie-Rehabilitation positiv beeinflussen.
Text
Hintergrund
Dysphagie-Patienten haben ein erhöhtes Risiko für eine Schlaganfall-assoziierte Pneumonie (SAP), die mit einer höheren Sterblichkeit und schlechterem neurologischem Outcome korreliert [1], [2], [3]. Die Wahrscheinlichkeit einer SAP wird durch die Faktoren Alter, Vorhofflimmern, Dysphagie, männliches Geschlecht und Schwere des Schlaganfalls beeinflusst, die im A2DS2-Score erfasst werden [4]. Ziel unserer bizentrischen Studie war es, die Auswirkung diätetischer Einschränkungen, insbesondere nil per os (NPO) und texturmodifizierter Kost (TMF), auf die Verringerung der SAP-Inzidenz bei Dysphagie nach Schlaganfall zu untersuchen.
Material und Methoden
Die Daten von 160 konsekutiven Patienten wurden retrospektiv ausgewertet: 73 Männer (Spanne 22-95 Jahre, Median 79) und 87 Frauen (Spanne 50-101 Jahre, Median 84). Die Betroffenen wurden auf zwei Schlaganfallstationen mit einer Gesamtkapazität von jeweils 20 Betten behandelt. Das primäre Outcome war die SAP-Inzidenz, während die Dauer des Krankenhausaufenthalts, die Sterblichkeit und die Notwendigkeit einer nasogastralen Sondenanlage zu den sekundären Outcomes gehörten.
Ergebnisse
Von den 160 Patienten der Gesamtkohorte wurde bei 54 Patienten (34%) eine SAP diagnostiziert, während die übrigen 106 Patienten (66%) mit ebenso initial auffälliger klinischer Schluckuntersuchung und Dysphagie keine SAP entwickelten. Die Ergebnisse zeigten eine starke Korrelation zwischen dem A2DS2-Score und der SAP-Wahrscheinlichkeit (p<0,001), wobei jeder Punktwert mehr die Wahrscheinlichkeit um 43,4% erhöhte (OR=1,434). Die Schwere des Schlaganfalls, das männliche Geschlecht und das Alter waren signifikante SAP-Risikofaktoren. Bei Aufnahme erhielten 63% der SAP-Patienten bereits NPO, 33% TMF, und nur 4% hatten keine Einschränkungen bei der oralen Nahrungsaufnahme. NPO-Patienten hatten ein 2,5-mal höheres Risiko, eine SAP zu entwickeln als Patienten ohne Ernährungseinschränkungen (p=0,008). Die Mehrzahl der SAP-Diagnosen wurde vor Beginn der oralen Nahrungsaufnahme gestellt, wobei die meisten Fälle bis zum dritten Tag entdeckt wurden.
Die unterschiedlichen Verläufe der Ernährungsempfehlungen für Patienten mit und ohne SAP sind in Abbildung 1 [Abb. 1] dargestellt. Im Sankey-Diagramm ist die Breite der farbigen Bänder proportional zur Anzahl der Patienten mit verschiedenen Ernährungsstrategien über die Dauer ihrer stationären Liegezeit. Dies verdeutlicht, dass NPO unter allen Ernährungsregimen den größten Beitrag zur SAP leistet.
Abbildung 1: Verschiedene Ernährungsstrategien nach der initialen klinischen Schluckuntersuchung (links) und bei Entlassung (rechts) in der Gesamtkohorte, mit Visualisierung der Veränderungen im Laufe der Zeit und der SAP-Entwicklung. Abkürzungen: NDR – keine diätetischen Einschränkungen; NPO – nil per os; SAP – Schlaganfall-assoziierte Pneumonie; TMF – texturmodifizierte Nahrung 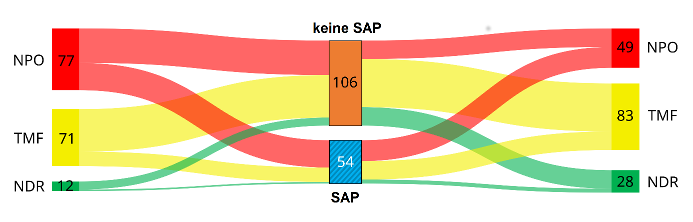
Abbildung 2 [Abb. 2] zeigt verschiedene laryngeale Befunde bei drei Patienten mit Dysphagie nach Schlaganfall unter NPO. Unverkennbar kann die laryngeale Funktion individuell unterschiedlich beeinträchtigt sein. Diese Befunde verdeutlichen die Notwendigkeit einer sorgfältigen endoskopischen Evaluation, um passgenaue therapeutische Maßnahmen für jeden einzelnen Patienten abzuleiten.
Abbildung 2: Laryngeale Befunde während der flexiblen endoskopischen Schluckuntersuchung (FEES) bei drei schluckgestörten Patienten nach Schlaganfall. Links: 65-jähriger Mann mit Pseudohypersalivation und Speichelaspiration. Mitte: 74-jährige Frau mit Aspiration von Nutilis aqua (IDDSI-Stufe 4). Rechts: 79-jähriger Mann mit beeinträchtigter Atemfunktion und trockenem, obstruktivem pharyngolaryngealem Sekret. 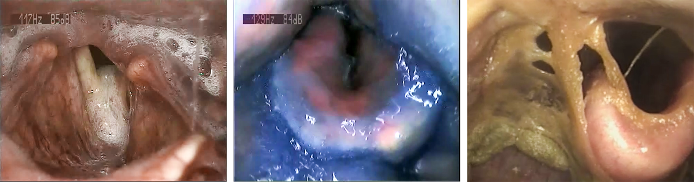
Bezüglich der sekundären Outcome-Parameter hatten Patienten mit SAP signifikant höhere stationäre Krankenhausaufenthaltsdauern (p<0,001) und Inzidenzen von nasogastralen Ernährungssonden (p<0,05) im Vergleich zu Patienten ohne SAP. Insgesamt starben 20% der Gesamtkohorte (32/160), wobei 28% in der SAP-Gruppe (15/54) und 16% in der Nicht-SAP-Gruppe (17/106) betroffen waren (p<0,079). Von den verstorbenen Patienten hatten 47% (15/32) eine Lungenentzündung erlitten. Ihr Durchschnittsalter lag bei 86 ± 8 Jahren (Mittelwert ± SD) und damit deutlich höher als das der überlebenden Probanden (78 ± 13, p=0,003).
Diskussion und Fazit
Trotz NPO zur Vorbeugung von Lungenentzündungen entwickelten viele Patienten dennoch eine SAP, was auf einen Einfluss von Mundhygienefaktoren und/oder systemischen und lokalen Immunveränderungen auf die pulmonale bakterielle Abwehr hindeutet. Unsere Studie unterstreicht die Notwendigkeit eines frühzeitigen Eingreifens und umfangreicher Pflegestrategien zur Minderung des SAP-Risikos bei Dysphagie-Patienten nach Schlaganfall. Geeignete Dysphagie-Diäten, die das residuale Schluckvermögen verbessern, könnten sowohl die SAP-Raten als auch die Dysphagie-Rehabilitation positiv beeinflussen.
References
[1] Dziewas R, Michou E, Trapl-Grundschober M, Lal A, Arsava EM, Bath PM, Clavé P, Glahn J, Hamdy S, Pownall S, Schindler A, Walshe M, Wirth R, Wright D, Verin E. European Stroke Organisation and European Society for Swallowing Disorders guideline for the diagnosis and treatment of post-stroke dysphagia. Eur Stroke J. 2021 Sep;6(3):LXXXIX-CXV. DOI: 10.1177/23969873211039721[2] Martino R, Foley N, Bhogal S, Diamant N, Speechley M, Teasell R. Dysphagia after stroke: incidence, diagnosis, and pulmonary complications. Stroke. 2005 Dec;36(12):2756-63. DOI: 10.1161/01.STR.0000190056.76543.eb
[3] Chang MC, Choo YJ, Seo KC, Yang S. The Relationship Between Dysphagia and Pneumonia in Acute Stroke Patients: A Systematic Review and Meta-Analysis. Front Neurol. 2022 Mar 17;13:834240. DOI: 10.3389/fneur.2022.834240
[4] Hoffmann S, Malzahn U, Harms H, Koennecke HC, Berger K, Kalic M, Walter G, Meisel A, Heuschmann PU; Berlin Stroke Register and the Stroke Register of Northwest Germany. Development of a clinical score (A2DS2) to predict pneumonia in acute ischemic stroke. Stroke. 2012 Oct;43(10):2617-23. DOI: 10.1161/STROKEAHA.112.653055




