Deutscher Rheumatologiekongress 2025
Deutscher Rheumatologiekongress 2025
Alles progrediente SSc-ILD, oder was?
Text
Vorgeschichte: Bei einer 60-jährigen Patientin wurde im Juli 2024 die Diagnose einer systemischen Sklerose (klinisch limitiert, ANA/anti-Scl70-AK pos.) mit initialer pulmonaler Manifestation (NSIP-Muster) gestellt, und eine Immunsuppression mit MMF 2x1.000 mg eingeleitet (Abbildung 1A [Fig. 1]).
Abbildung 1: 1A: Thorax-CT bei Diagnosestellung SSc-ILD, 1B: Thorax-CT bei ARDS, 1C: Thorax-CT am Ende der Ganciclovir-Therapie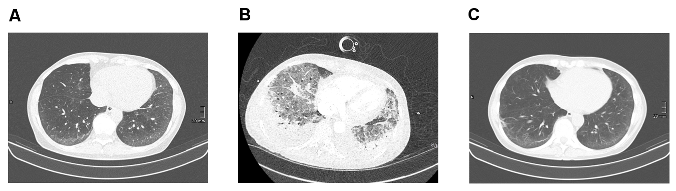
Leitsymptome bei Krankheitsmanifestation: Im Oktober 2024 wurde die Patientin wegen progredienter Belastungsdyspnoe, Fieberschübe und AZ-Verschlechterung stationär aufgenommen. In der klinischen Untersuchung zeigten sich eine diffuse Schwellung der Hände im Sinne von „puffy fingers“ sowie eine deutliche Hautsklerose (mRSS 10 Punkte), über beiden Lungenflügeln war auskultatorisch basales Knistern festzustellen.
Diagnostik und Verlauf: Laborchemisch bestand eine systemische Inflammation (CRP-Wert initial 36 mg/l) bei normwertigem PCT-Wert. Im Routinelabor war ein deutlich erhöhter LDH-Wert auffällig (506 IU/l). Im CT-Thorax fand sich eine deutl. Zunahme der interstitiellen Lungenveränderungen mit neuer Milchglaskomponente. Neben einem Progress der SSc-ILD wurde insbesondere auch an eine infektiöse Genese der Lungenveränderungen gedacht. Die MMF-Therapie wurde beendet und eine umfangreiche mikrobiologische Diagnostik veranlasst. In PCR-Analysen des Rachenspülwassers fand sich ein schwach positiver Befund für CMV-DNA (6,2 x102 Kopien/ml) bei unauffälligen Befunden für Pneumocystis, HSV1/2, Influenza A/B, Parainfluenza I-III, RSV, HMPV und Adenovirus. Es wurde eine Therapie mit Ganciclovir i.v. initiiert sowie bei klinischer und laborchemischer Verschlechterung (Anstieg von CRP auf 176 mg/l, PCT auf 1,6 ng/ml und LDH auf 909 IU/l) eine rasche Bronchoskopie mit BAL durchgeführt. In der BAL konnte eine deutlich höhere Kopienanzahl von CMV-DNA nachgewiesen werden (8x104), die weiteren Multiplex-Analysen bzw. Kulturen auf resp. Erreger blieben vollständig negativ. Weitere PCR-Analysen zeigten auch positive Befunde für CMV-DNA im Blut (9,9x105 Kopien/ml) und Stuhl (3,2x102 Kopien/ml). Die CMV-Serologie ergab positive Titer für CMV-spezifische IgM- und IgG-AK, wobei für die IgG-AK nur eine sehr geringe Avidität gemessen wurde (2,9%). Trotz der Ganciclovirtherapie entwickelte die Pat. ein ARDS und musste intensivmedizinisch versorgt werden (Abbildung 1B [Fig. 1]). Unter einer fortgesetzten Ganciclovirtherapie, invasiven Beatmung und Bauchlagerung gelang eine Stabilisierung und im Verlauf Besserung der resp. Situation. Konsekutive PCR-Analysen zeigten abfallende und im Verlauf negative Befunde für CMV-DNA in der BAL, im Blut und im Stuhl. Wiederholte Serologien zeigten einen Anstieg der Avidität der CMV-spezifischen IgG-AK bis auf 35,1%. In einem Verlaufs-CT konnte eine vollständige Rückbildung der akut entzündlichen Lungenveränderungen bei unveränderten Befunden der SSc-ILD dokumentiert werden (Abbildung 1C [Fig. 1]). Die im Verlauf auf orales Valganciclovir umgestellte Therapie konnte deshalb 01/2025 beendet und bei weiterhin stabilem Verlauf die Immunsuppression mit MMF 03/2025 bei SSc-ILD wieder aufgenommen werden. Nach einer Rehabilitationsmassnahme kann sich die Patientin inzwischen wieder intensiv sportlich betätigen (Skitourengehen).
Diagnose: Akutes Lungenversagen bei CMV-Pneumonitis im Rahmen einer Primärinfektion unter immunsuppressiver Therapie mit MMF bei SSc-ILD.
Diskussion: Üblicherweise findet eine CMV-Infektion bis ins junge Erwachsenenalter statt (Durchseuchung in Industrieländern bei Erwachsenen ca. 80%), so dass der Nachweis von CMV-DNA bei erwachsenen Patienten unter einer Immunsuppression in den meisten Fällen auf eine CMV-Reaktivierung zurückzuführen ist. Bei unserer Patientin ist allerdings von einer primären CMV-Infektion auszugehen. Hierfür spricht insbesondere die initial dokumentierte niedrige Avidität der CMV-spezifischen IgG-Antikörper, was typisch für die Frühphase einer Infektion ist, und die später deutlich ansteigende Avidität der CMV-spezifischen IgG-AK als Ausdruck eines Reifungsprozesseses im Rahmen der primären Immunantwort. Auch der sehr schwere Verlauf der CMV-Infektion mit hohen Kopienzahlen und eine anamnestisch durch die Betreuung von Kleinkindern (Enkel) mit häufigem Windelwechseln bestehende potenzielle CMV-Exposition sprechen bei unserer Patientin für eine seltene CMV-Primärinfektion im Erwachsenenalter.
Offenlegungserklärung: Die Autoren erklären, dass keine Interessenkonflikte bestehen.




