Deutscher Rheumatologiekongress 2025
Deutscher Rheumatologiekongress 2025
Einfluss der Immunphänotypisierung auf die Therapiepersistenz bei Psoriasis-Arthritis
Text
Einleitung: Biologic Disease-Modifying Anti-Rheumatic Drugs (bDMARDs) sind eine gängige Therapie für Psoriasis-Arthritis (PsA), jedoch existiert bisher keine etablierte Methode zur individuellen Auswahl des am besten geeigneten bDMARDs. Personalisierte Medizin könnte hier einen vielversprechenden Ansatz bieten. Ziel unserer Studie ist die Entwicklung eines Algorithmus, basierend auf Immunphänotypisierung, der die Identifikation des am besten geeigneten bDMARDs für jeden Patienten unterstützt und somit Therapiepersistenz und -ansprechen verbessert. Ein vergleichbarer Ansatz wurde von Miyagawa, Nakayamada et al. [1] bereits beschrieben. Hier präsentieren wir die ersten Ergebnisse unserer Studie, die Teil eines laufenden multizentrischen Projekts an den Zentren für Personalisierte Medizin in Baden-Württemberg ist.
Methoden: Wir führten eine Immunphänotypisierung bei 31 Erstlinienpatienten mit PsA durch. Davon wurden 18 Patienten nach einem Algorithmus (AL) mit bDMARDs therapiert, der auf phänotypischen Unterschieden in peripheren T-Helfer-Zellen basiert, welche mittels 8-Farben-Durchflusszytometrie analysiert wurden (Miyagawa et al. [1]). 13 Patienten erhielten eine Therapie mit bDMARDs nach individueller ärztlicher Entscheidung (PC). Die Therapiepersistenz wurde über einen Zeitraum von 31 Wochen verglichen.
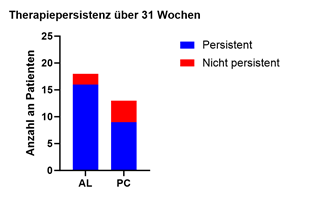
Ergebnisse: Die AL-Gruppe wurde in vier Immunphänotypen unterteilt: aktivierter Th1-Zell-dominanter, aktivierter Th17-Zell-dominanter, Th1/Th17-high und Th1/Th17-low Typ (Miyagawa et al., 2019). Patienten erhielten entsprechend ihrem Phänotyp folgende bDMARDs: Th1-dominante Patienten Ustekinumab, Th17-dominante sowie Th1/Th17-high Patienten Interleukin-17- oder -23-Inhibitoren, und Th1/Th17-low Patienten TNF-Inhibitoren. Von den 18 nach Algorithmus behandelten Patienten blieben 16 (88,9%) über einen Zeitraum von mindestens 31 Wochen therapiepersistent, während zwei (11,1%) einen Therapieabbruch oder -wechsel zeigten. In der PC-Gruppe blieben neun von 13 Patienten (69,2%) über 31 Wochen therapiepersistent, während vier (30,8%) nicht persistent waren (nicht signifikant, p = 0,2076, exakter Test nach Fisher).
Schlussfolgerung: Unsere Studie validierte den von Miyagawa et al. [1] beschriebenen Ansatz unter realen Bedingungen. Obwohl der Unterschied in der Therapiepersistenz nicht signifikant war, zeigt der Trend eine potenzielle Relevanz der phänotypbasierten Therapieentscheidung. Eine personalisierte Therapieempfehlung sollte auf einer Kombination mehrerer Parameter basieren, die in die Pathophysiologie der PsA involviert sind. Die Integration zusätzlicher diagnostischer Verfahren wie Proteomik oder Metabolomik könnte die Vorhersage des Therapieansprechens weiter verbessern. Der Ausbau des Netzwerks der Zentren für Personalisierte Medizin in Baden-Württemberg stellt eine entscheidende wissenschaftliche Expertise zur Validierung neuer Biomarker und Therapieansätze in multizentrischen, qualitätsgesicherten Studien.
Abbildung 1 [Fig. 1]
Abbildung 1: Therapiepersistenz über 31 Wochen Quelle: Eigene Darstellung