Deutscher Rheumatologiekongress 2025
Deutscher Rheumatologiekongress 2025
Schwangerschaftsverläufe und -komplikationen bei Frauen mit systemischem Lupus erythematodes – Vergleich von Register- und Krankenkassendaten
Text
Einleitung: Schwangerschaften von Frauen mit systemischem Lupus erythematodes (SLE) haben ein höheres Risiko für mütterliche und kindliche Komplikationen [1]. Die vorliegende Studie untersuchte Komplikationsraten in zwei Datenquellen: im Schwangerschaftsregister Rhekiss und in Abrechnungsdaten der BARMER Krankenkasse.
Methoden: In das bundesweite, multizentrische, webbasierte Rhekiss-Register werden Frauen mit verschiedenen entzündlich-rheumatischen Erkrankungen eingeschlossen, wenn sie eine Schwangerschaft planen oder bereits schwanger sind. Daten werden von behandelnden Rheumatolog:innen sowie Patientinnen zu regelmäßigen Messzeitpunkten dokumentiert. Für diese Analyse wurden Frauen mit SLE und einer Einlingsschwangerschaft zwischen 2015–2023 untersucht. Aus den BARMER-Abrechnungsdaten wurden Frauen im Alter von 18–55 Jahren mit ≥2 ambulanten oder ≥1 stationären SLE-Diagnose(n) innerhalb von 12 Monaten in den Jahren 2005–2023 ausgewählt. Einlingsschwangerschaften/-geburten wurden über ICD-10-Codes, Gebührenordnungs-positionen des einheitlichen Bewertungsmaßstabes und Operationen- und Prozedurencodes identifiziert [2]. Komorbiditäten wurden im Kalenderjahr vor Empfängnis und Schwangerschaftskomplikationen zwischen geschätzter Empfängnis und 8 Wochen nach Schwangerschaftsausgang untersucht. Alle Daten wurden deskriptiv analysiert.
Ergebnisse: Insgesamt wurden 1.205 Einlingsschwangerschaften ausgewertet, n=325 aus den Register- und n=880 aus den Abrechnungsdaten. Das Alter der Frauen war in beiden Datenquellen vergleichbar (Tabelle 1 [Tab. 1]), aber die Frauen aus dem Register wiesen eine höhere Krankheitslast auf, mit längerer Krankheitsdauer und häufigerem Vorkommen von Autoimmunthyreoiditis, Antiphospholipid-Syndrom und Glomerulonephritis. Während Schwangerschaftskomplikationen wie Präeklampsie/HELLP häufiger in den Abrechnungsdaten registriert wurden (11,3% vs. 2,8%), zeigten die Registerdaten eine höhere Fehlgeburtenrate (5,6% vs. 0,2%), Tabelle 2 [Tab. 2]. Der Anteil an Lebendgeburten war vergleichbar (93% vs. 94%).
Table 1: Charakteristika der Schwangerschaften.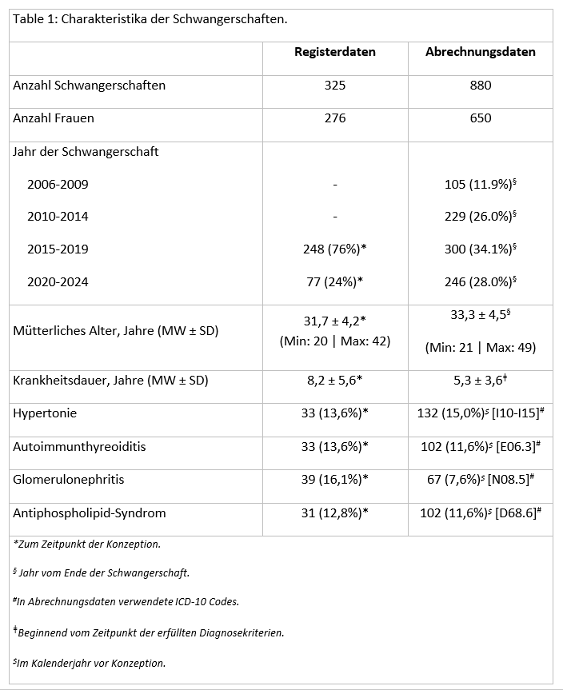
Table 2: Schwangerschaftskomplikationen und -ausgang.
Schlussfolgerung: Beide Datenquellen haben individuelle Vor- und Nachteile. Das Rhekiss-Register umfasst detaillierte klinische Informationen und repräsentiert eine von Rheumatolog:innen betreute Population, mit meist geplanten Schwangerschaften und aktiver Schwangerschaftsberatung (78%). Im Gegensatz dazu bieten Abrechnungsdaten eine breitere, bevölkerungsbezogene Perspektive, dafür aber keine klinischen Details.
Die Register-Patientinnen zeigten eine höhere Krankheitslast, erzielten aber dennoch günstige Schwangerschaftsoutcomes, was möglicherweise auf eine optimale Versorgung und eine gut kontrollierte Krankheitsaktivität zurückzuführen ist (mittlere Krankheitsaktivität [Arzt-berichtet, 0–10]: 1,5±1,4). In den Abrechnungsdaten waren Schwangerschaftskomplikationen häufiger. Die ähnliche Lebendgeburtenrate in beiden Datenquellen zeigt, dass ein guter Schwangerschaftsverlauf und -ausgang auch bei SLE-Patientinnen mit schwerer Erkrankung möglich ist.
Weitere geplante Analysen umfassen SLE-Therapien, Inanspruchnahme von Fachärzt:innen und neonatale Charakteristika, um die Auswirkungen der Versorgung auf Unterschiede in den Ergebnissen besser zu verstehen.
Literatur
[1] Bundhun PK, Soogund MZ, Huang F. Impact of systemic lupus erythematosus on maternal and fetal outcomes following pregnancy: A meta-analysis of studies published between years 2001-2016. J Autoimmun. 2017 May;79:17-27. DOI: 10.1016/j.jaut.2017.02.009[2] Mikolajczyk RT, Kraut AA, Garbe E. Evaluation of pregnancy outcome records in the German Pharmacoepidemiological Research Database (GePaRD). Pharmacoepidemiol Drug Saf. 2013 Aug;22(8):873-80. DOI: 10.1002/pds.3467




