Deutscher Rheumatologiekongress 2025
Deutscher Rheumatologiekongress 2025
Anwendung von biologischen krankheitsmodifizierenden Antirheumatika und Januskinase-Inhibitoren bei juveniler idiopathischer Arthritis: Daten aus dem BIKER-Register 2000–2024
Text
Einleitung: Biologische krankheitsmodifizierende Antirheumatika (bDMARDs) haben die Behandlung der juvenilen idiopathischen Arthritis (JIA) revolutioniert und gezielte Therapien für Kinder mit mittelschwerer bis schwerer Erkrankung ermöglicht. Diese Studie untersucht die sich wandelnde Rolle von Biologika und Januskinase-Inhibitoren (JAKi) in der pädiatrischen Rheumatologie in Deutschland über die vergangenen 25 Jahre anhand von Daten aus dem BIKER-Register [1].
Methoden: Diese Studie analysiert die Trends in der Anwendung von bDMARDs und JAK-Inhibitoren bei JIA in Deutschland (2000–2024) und vergleicht deren Nutzung in verschiedenen JIA-Kategorien, darunter polyartikuläre JIA (pJIA), systemische JIA (sJIA), Enthesitis-assoziierte Arthritis (ERA), juvenile Psoriasis-Arthritis (jPsA) und persistierende Oligoarthritis (pOJIA) bei Kindern.
Dazu wurde eine retrospektive Kohortenanalyse mithilfe von Daten aus dem BIKER-Register (2000–2024) durchgeführt. Die Analyse umfasste 6.263 Therapieinitiierungen bei 4.195 Patienten. Zeitliche Trends in der Therapieanwendung wurden mittels deskriptiver Statistiken und grafischer Darstellungen bewertet.
Ergebnisse: Etanercept war bis 2007 mit über 90% der Anwendungen das dominierende bDMARD, wurde jedoch 2023 von Adalimumab abgelöst (29% vs. 26%, Abbildung 1 [Fig. 1]). Trotz dieser Verschiebung blieb die TNF-Inhibition in den letzten fünf Jahren mit durchschnittlich 72% der bDMARD-Nutzung die zentrale Therapieklasse. Neuere Therapieoptionen, darunter IL-6-Inhibitoren (17%) und JAK-Inhibitoren (6%), wurden in geringerem Umfang eingesetzt. Bei pJIA blieben TNFi die primäre Therapie. Abatacept als CTLA-4-Fusionsprotein wurde nur in geringem Umfang eingesetzt, während JAK-Inhibitoren im Jahr 2022 mit 24% der Initiierungen ihren bisherigen Höchststand erreichten (Abbildung 2A [Fig. 2]). Für sJIA wandelten sich TNFi von der einzigen Therapieoption zu keinen neuen Initiierungen mehr. Während TNFi bis 2009 noch 54% der Therapiestarts ausmachten, nahm ihre Nutzung stetig ab und wurde durch IL-1- und IL-6- Inhibitoren ersetzt (Abbildung 2C [Fig. 2]). In der ERA/PsA-Gruppe dominierten TNFi weiterhin, während JAK-Inhibitoren und IL-17-Inhibitoren zusammen durchschnittlich 23% der neuen Behandlungen ausmachten (Abbildung 2B [Fig. 2]). Bei pOJIA behielten TNFi einen dominanten Anteil an den Therapieinitiierungen. In den letzten Jahren gewannen IL-6-Inhibitoren zunehmend an Bedeutung und machen mittlerweile etwa 25% der neuen Behandlungen aus (Abbildung 2D [Fig. 2]).
Abbildung 1: Prozentsatz der Patienten mit juveniler idiopathischer Arthritis (JIA), die in den jeweiligen Jahren biologische DMARDs erhielten, sowie Zulassungsdaten der jeweiligen Wirkstoffe in Europa (2000–2024)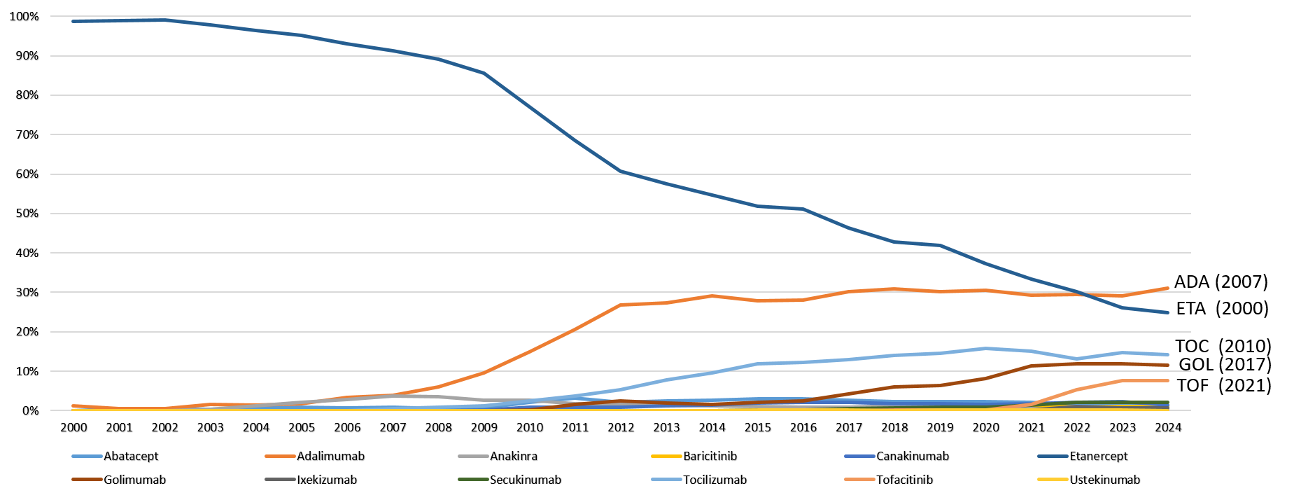
Abbildung 2: Initiierung von biologischen DMARDs und JAK-Inhibitoren bei Patienten mit polyartikulärer JIA (pJIA), systemischer JIA (sJIA), Enthesitis-assoziierter Arthritis (ERA), juveniler Psoriasis-Arthritis (jPsA) und persistierender Oligoarthritis (pOJIA) (in %)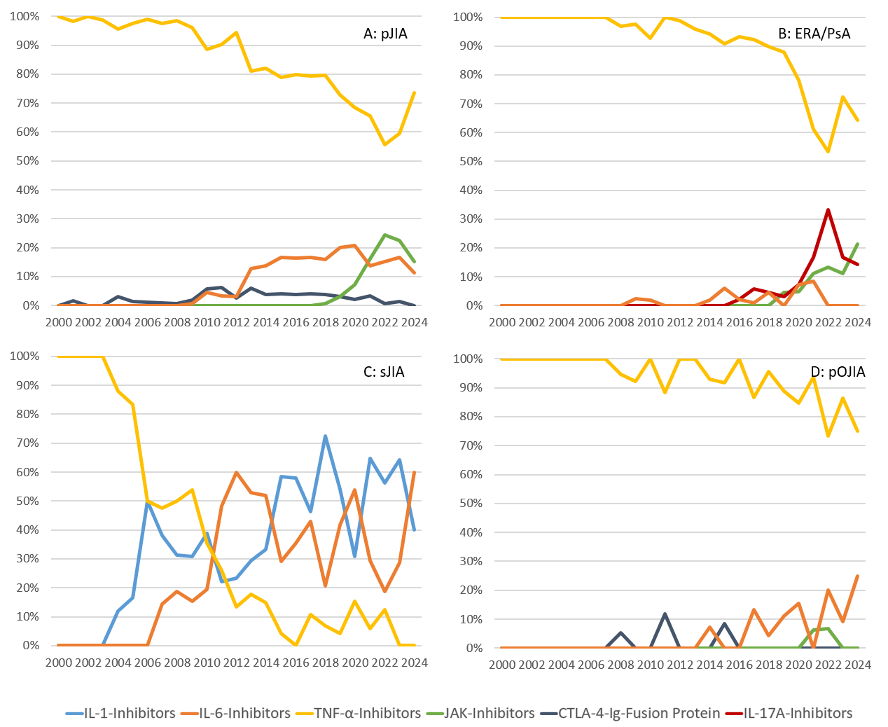
Schlussfolgerung: In den letzten 25 Jahren blieben TNF-alpha-Inhibitoren die zentrale Säule der JIA-Therapie. Neue Biologika wie IL-6-Inhibitoren, JAK-Inhibitoren und IL-17A-Inhibitoren konnten die Behandlungsmöglichkeiten jedoch inzwischen deutlich erweitern, insbesondere für komplexe JIA-Formen.




