German Congress of Orthopaedics and Traumatology (DKOU 2025)
Deutscher Kongress für Orthopädie und Unfallchirurgie 2025 (DKOU 2025)
Vergleich des Effektes von Mangan- und Kupfersupplementation in mesoporösen bioaktiven Glasnanopartikeln auf die Expression angiogener Wachstumsfakturen von mesenchymalen Stromazellen in vitro und Gefäßneubildung in ovo
Text
Zielsetzung und Fragestellung: Mesoporöse bioaktive Nanopartikel (MBGNs; Zusammensetzung in wt%: 70 SiO2 und 30 CaO) können als vielversprechendes Knochenersatzmaterial mit Ionen supplementiert werden, um ihre biologischen Eigenschaften und somit auch therapeutisches Potenzial in der Behandlung von Knochendefekten zu modifizieren. Neben einer Modifikation möglicher osteogener Eigenschaften sind angiogene Effekte zur verbesserten Nährstoffversorgung vorteilhaft. Vielversprechende Ionen hierfür sind Mangan (Mn) und Kupfer (Cu). Vergleichend soll der Einfluss dieser als Bestandteil von MBGNs auf die Expression von angiogenesefördernden Proteinen durch mesenchymale Stromazellen (MSCs) in vitro sowie der Gefäßneubildung in ovo evaluiert werden.
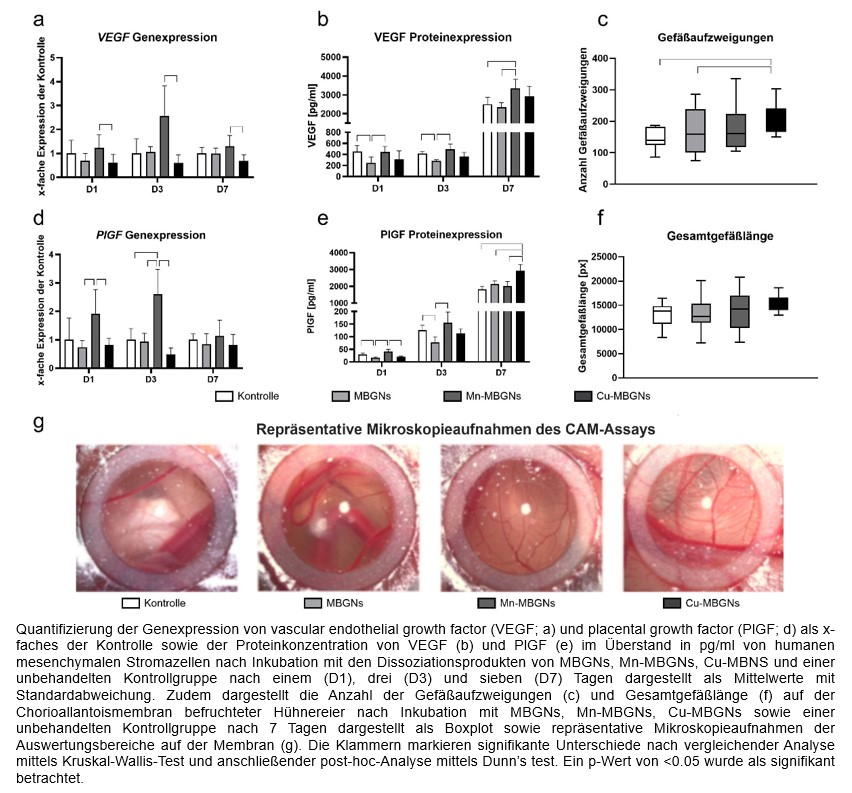
Material und Methoden: MBGNs, sowie Mn- und Cu-supplementierte MBGNs (Zusammensetzung in wt%: 5Mn-MBGNs: 70 SiO2, 25 CaO, 5 MnO; 5Cu-MBGNs: 70 SiO2, 25 CaO, 5 CuO) wurden in einer Konzentration von 0,4 mg/ml zu Zellkulturmedium gegeben. MSCs wurden über einen (D1), drei (D3) und sieben (D7) Tage mit in den Überständen befindlichen Dissoziationsprodukten von BG-supplementiertem Medium sowie BG-freiem Medium (Kontrollgruppe) kultiviert. An den Auswertungstagen wurden sowohl auf Ebene der Genexpression mittels qPCR, als auch auf Ebene der Proteinexpression mittels ELISA die Expressionsniveaus von vascular endothelial growth factor (VEGF) und placental growth factor (PlGF) bestimmt. Zudem erfolgte die Gabe von 120 µg der jeweiligen MBGNs auf die Chorioallantoismembran (CAM) befruchteter Hühnereier. An D7 erfolgte die Quantifizierung der Gefäßaufzweigungen und Gesamtgefäßlänge auf der CAM.
Ergebnisse: Insbesondere an D3 zeigte sich eine bis zu 2,5-fach erhöhte Expression von VEGF und PlGF der MSCs in der Mn-MBGN- gegenüber der MBGN- und Kontrollgruppe. Diese zeigte sich weiterhin an D7, sowie geringer ausgeprägt auf Ebene der Proteinexpression.
In Kontakt zu den Dissoziationsprodukten der Cu-MBGNs zeigte sich keine Erhöhung der Genexpression der untersuchten Marker. Jedoch lagen die Maximalwerte der Proteinexpression von PlGF in der Cu-MBGN-Gruppe an D7. Auch die VEGF-Proteinexpression zeigte sich hier gegenüber den weiteren Versuchsgruppen erhöht.
Im CAM-Assay zeigten sich sowohl für Mn-MBGNs als auch für Cu-MBGNs angiogenesefördernde Eigenschaften. Bei Betrachtung der Anzahl der Gefäßaufzweigungen sowie der Gesamtgefäßlänge zeigten sich Maximalwerte mit signifikanter Erhöhung gegenüber der Kontrollgruppe in Kontakt zu Cu-MBGNs. Ebenso zeigte sich die Gesamtgefäßlänge in der Mn-MBGN-Gruppe gegenüber den weiteren Versuchsgruppen erhöht.
Diskussion und Schlussfolgerung: Sowohl Mn-MBGNs in vitro als auch Cu-MBGNs in ovo zeigten angiogenenefördernde Effekte. Weitere Untersuchungen unter verlängerter Inkubationszeit oder unter direktem Kontakt der MBGNs in vitro könnten weiteren Aufschluss über das angiogene Potenzial der Ionensupplementation in MBGNs bringen. Sollten sich hier die angiogenesefördernden Eigenschaften bestätigen, stellen ionensupplementierte MBGNs vielversprechende Kandidaten für eine perspektivische in vivo Untersuchung in Knochendefektmodellen dar.
Abbildung 1 [Fig. 1]